电池工作原理
电池的工作原理是电解液与金属的氧化和还原反应。当两种不同的称为电极的金属物质置于稀释的电解液中时,根据电极中金属的电子亲和度,电极中分别发生氧化和还原反应。由于氧化反应,一个电极带负电荷称为阴极,由于还原反应,另一个电极带正电荷称为阳极。
电池的阴极是负极,而阳极是正极。了解电池基本原理正确地说,首先,我们应该有一些电解质和电子亲和能的基本概念。实际上,当两种不同的金属浸在电解液中,就会有潜在的差异在这些金属之间产生的。
人们发现,当一些特定的化合物被添加到水中时,它们会溶解并产生负离子和正离子。这种化合物被称为电解质。电解质的常见例子几乎是各种盐、酸、碱等。中性原子接受电子时所释放的能量称为电子亲和能。随着原子结构由于不同的材料是不同的,不同材料的电子亲合力也会不同。
如果两种不同的金属浸入同一电解质溶液中,其中一种会获得电子,另一种会释放电子。哪一种金属(或金属化合物)将获得电子,哪一种将失去电子,取决于这些金属的电子亲合力。低电子亲和能的金属将从电解质溶液的负离子中获得电子。
另一方面,具有高电子亲和能的金属会释放电子,这些电子进入电解质溶液,加入溶液中的正离子。这样,一种金属得到电子,另一种失去电子。因此,这两种金属之间的电子浓度会有差异。
这种电子浓度的差异导致金属之间产生电位差。这种电位差或电动势可被用作电势电压源在任何电子产品yabo和365哪个平台更大或电路。这是一般的和基本的电池原理这是电池的工作原理。
所有的电池都是基于这一基本原理。让我们逐一讨论。就像我们之前说的,亚历山德罗·沃尔塔发明了第一个电池,这个电池通常被称为简单电池伏打电池。创建这种类型的简单单元格非常容易。取一个容器,装满稀释的硫酸作为电解液。现在,我们将一根锌和一根铜棒浸入溶液中,然后通过一个电力负载将它们连接到外部。现在你简单的电池完成了。电流将开始流过外部负载。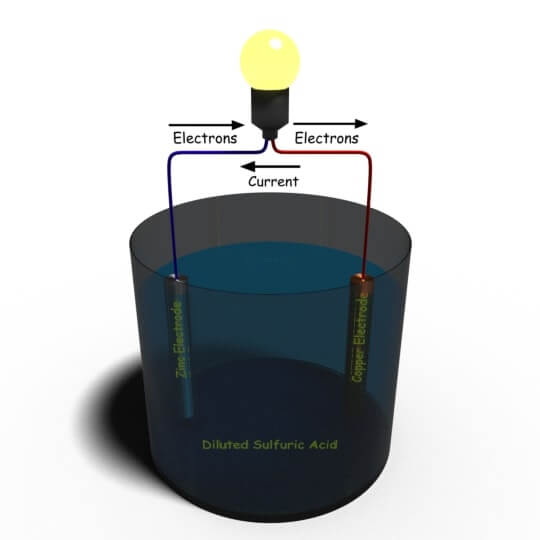
在稀硫酸中,锌释放出的电子如下: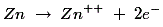
这些锌+ +离子进入电解质,而每个Zn+ +离子在棒中留下两个电子。由于上述氧化反应,锌电极是留下负电荷,因此作为一个阴极。因此,锌的浓度+ +电解质中接近阴极的离子增加。
根据电解液的性质,稀释后的硫酸和水已经分解成正的水合氢离子和负的硫酸离子,分别如下: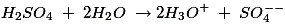
由于锌的浓度很高+ +靠近阴极H的离子3.O+离子被排斥到铜电极,通过吸收铜棒原子中的电子而被释放。以下反应发生在阳极上: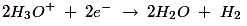
由于还原反应发生在铜电极上,铜棒得到正电荷,因此它充当阳极。
丹聂耳电池
的丹聂耳电池由含有硫酸铜溶液的铜容器组成。铜容器本身充当正极。在铜容器中放入一个装有稀硫酸的多孔锅。一个浸在硫酸中的锌合金棒作为负极。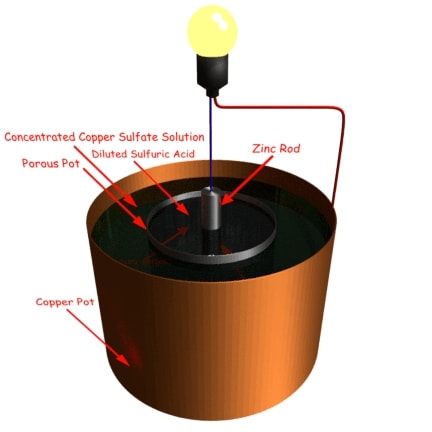
稀释的硫酸在多孔锅中与锌反应,从而使氢得到细化。反应过程如下: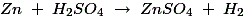
ZnSO的形成4在多孔锅中,ZnSO结晶后才影响胞体的工作4沉积。氢气通过多孔锅与CuSO反应4解决方案如下: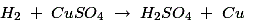
这样形成的铜会沉积在铜容器上。
炮台的历史
1936年仲夏,在伊拉克巴格达市附近,人们在修建新铁路线时发现了一座古墓。在那个坟墓中发现的文物大约有两千年的历史。在这些遗物中,有一些用沥青密封在顶部的陶罐。一根铁棒,周围有一根用铜片包裹的圆柱形管子,从密封的顶部伸出来。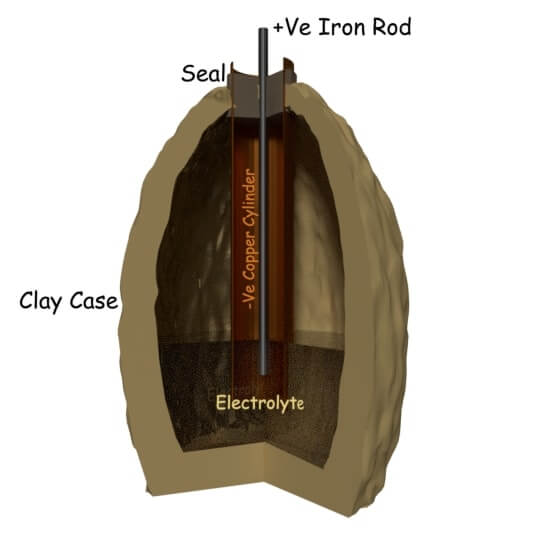
当发现者用酸性液体填充这些罐子时,他们发现铁和铜之间的电位差约为2伏。这些陶罐被怀疑是2000年前的电池。他们把这个罐子命名为帕提亚的电池。
1786年,意大利解剖学家兼生理学家路易吉·加瓦尼惊讶地发现,当他用两种不同的金属触摸死去的青蛙腿时,腿上的肌肉收缩了。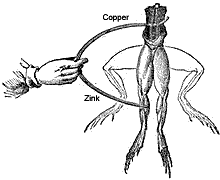
他不明白真正的原因,否则他就会被称为电池的第一个发明者。他认为这种反应可能是由于组织的某种性质。

在那之后,亚历山德罗·沃尔塔发现同样的现象出现在浸泡在盐水中的纸板上,而不是青蛙腿上。他把一个铜盘和一个锌盘夹在一起,中间夹着一块浸在盐水里的硬纸板potential区别在铜和锌之间。
在那之后的1800年,他开发了第一个电池(电池)由交替的铜和锌盘组成,中间是浸泡在盐水中的纸板。这个系统可以产生可测量的电流。我们认为Alessandro Volta的Voltaic作为第一个“湿电池”。因此,电池的历史开始了。从那时起直到今天,电池仍然是首选的电力来源。在我们的许多日常生活中应用。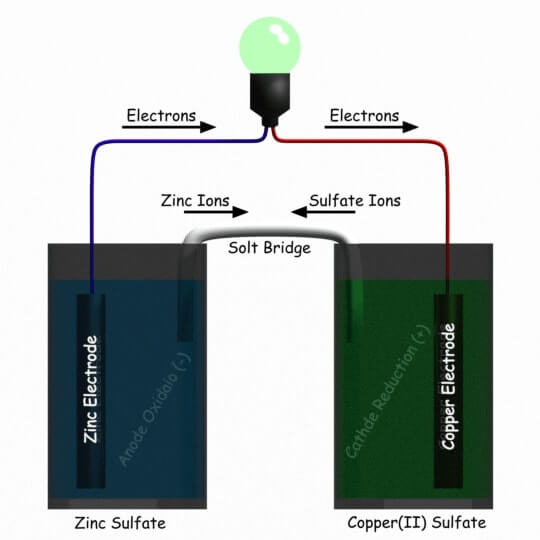
光伏发电桩的主要问题是它不能长时间输送电流。英国发明家约翰·f·丹尼尔在1836年解决了这个问题。他发明了一种更先进的电池被称为丹聂耳电池。约翰·f·丹尼尔将一根锌棒浸入一个容器中的硫酸锌中,将一根铜棒浸入另一个容器中的硫酸铜(II)中。
一个U形的盐桥连接着这两个容器的溶液。一个丹尼尔电池可以产生1.1伏电压,而且这种类型的电池比伏打电池持续时间长得多。1839年,发现者、科学家威廉·罗伯特·格罗夫爵士设计了燃料电池。他将氢和氧混合在电解质溶液中,产生了电和水。燃料电池没有提供足够的能量,但它是有用的。本生(1842年)和格罗夫(1839年)发明了使用液体电极供电的电池。

1859年,加斯顿·普兰特;率先研制出铅酸蓄电池。铅酸蓄电池是可充电二次电池的第一种形式。铅酸电池仍在许多工业用途中使用。它仍然是最常用的汽车电池。1866年,一位法国工程师,乔治·勒朗什,开发了一种新型电池。这是一种碳锌湿电池勒克朗谢电池。
压碎的二氧化锰与少量碳混合形成正极,锌棒形成负极。他用氯化铵溶液作为液体电解质。几年后,乔治·勒布兰奇自己改进了他的设计,用氯化铵代替液态氯化铵溶液。
因此,他发明了第一个干电池。1901年,托马斯·阿尔瓦·爱迪生发现碱性蓄电池。托马斯·爱迪生的原电池以铁作为正极材料(-),以镍氧化物作为正极材料(+)。以上内容只是无穷无尽的一部分电池的历史。
电池发展史上的一步一步发展
| 开发者/发明家 | 国家 | 一年 | 发明 |
| 路易吉伽尔伐尼 | 意大利 | 1786 | 动物电 |
| 伏打 | 意大利 | 1800 | 伏打电堆 |
| 约翰·f·丹尼尔 | 英国 | 1836 | 丹聂耳电池 |
| 威廉·罗伯特·格罗夫爵士 | 英国 | 1839 | 燃料电池 |
| 罗伯特本生 | 德国 | 1842 | 用液体电极供电 |
| 加斯顿普兰特 | 法国 | 1859 | 铅酸电池 |
| 乔治Leclanche | 法国 | 1866 | 勒克朗谢电池 |
| 托马斯·阿尔瓦·爱迪生 | 美国 | 1901 | 碱性蓄电池 |









