在1808年,着名的英国化学家,物理学家和气象学家John Dalton发表了他的理论原子。那时,许多未解释的化学现象被道尔顿理论迅速解锁。因此,该理论成为化学的理论基础。道尔顿原子理论的假设如下。
- 所有物质由称为原子的小不可分割和坚韧的颗粒组成。
- 同一种元素的所有原子具有相同的性质,但不同于其他元素的原子。
- 不同元素的原子组合在一起形成化合物。
- 化学反应只不过是这些原子的重新排列。
- 原子不能以任何方式创造或毁灭。
道尔顿的理论有一些弊端;今天我们知道原子可以被摧毁。而且,相同元素的一些原子在其质量(同位素)中变化。该理论也未能解释同种异体的存在。
但在Mordern Era的原子概念基于结合的优点Rutherford的原子模型和Bohr的原子模型。所有物质都由原子组成。所有原子包括,
- 核
- 电子
原子核心
原子核位于原子的中心。原子核的直径约为整个原子直径的万分之一。几乎整个原子的质量都集中在原子核里。原子核本身由两种粒子组成,
- 质子
- 中子
质子
质子是带正电的粒子。每个质子的电荷是1。6×10-19库仑。原子核中的质子的数量代表原子数的原子。
中子
中子没有电荷。意思是,中子是电中性颗粒。每个中子的质量等于质子的质量。
由于存在带正电荷的质子,核被带正电荷。在任何材料中,原子的重量和放射性特性与细胞核相关。
电子
电子是存在于原子中的带负电荷的粒子。每个电子电荷为-1.6×10- 19.库仑。这些电子环绕着细胞核。下面列出并解释了原子中的电子中的一些事实,
- 如果原子具有相同数量的质子和电子,则原子是电中性,因为电子的负电荷中和质子的正电荷。
- 电子围绕壳中的细胞核(也称为轨道)。
- 通过带正电荷的核,吸引力的吸引力排出带负电的电子。这种吸引力的力量适用于核周围电子革命所需的向量。
- 靠近核的电子与核紧密地结合,并且更难以比远离核的原子从原子中拉出(去除)这些电子。
- 铝原子的结构如下图所示
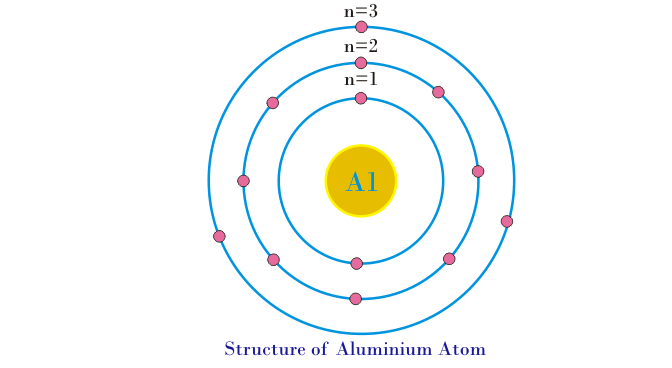
- 需要一定量的能量来从其轨道中除去电子。与第一轨道从第一轨道移除电子所需的能量比从外轨道移除电子所需的能量相比更多。这是由于与在外轨上的电子上排泄的吸引力相比,第一轨道上的核心的吸引力的吸引力要多得多。类似地,与第一个轨道相比,从第二轨道移除电子所需的能量将较少,并且大于第三轨道。因此,我们可以说轨道中的电子与明确的能量相关联。因此,轨道或壳也称为能量水平。
- 能量水平由字母k,l,m,n等表示。其中,k是核的最近轨道,并且能量水平最低。相反,最外面的轨道具有最高能量水平。
- '2N的任何能级中的最大电子数2',其中,n是整数,表示“主量子数”。对于不同的能量水平,下表中给出的“N”和最大电子数量
| SL。没有。 | 能量水平或轨道(壳) | 主量子数'n' | 最大电子数(2N2) |
| 1 | K. | 1 | 2×12= 2 |
| 2 | L. | 2 | 2×22= 8 |
| 3. | m | 3. | 2×32= 18 |
| 4. | N | 4. | 2×42= 32. |
- 上述公式(2N2)用于确定任何外壳中的最大电子数,具有一些限制。最外壳(最高能级)中的电子数不能超过8.例如,让我们考虑钙的原子,它在其核周围具有20个电子。根据上述规则的公式i.E.2N2,电子分布将在k电平中的2个电子,L电平8个电子,并且存在10个电子。但是,外部能量水平中的电子不能超过8.因此,M级中将存在8个电子,并且平衡2电子将进入下一个能级I.E.2电子将达到n水平。钙原子的电子配置如下图所示 -
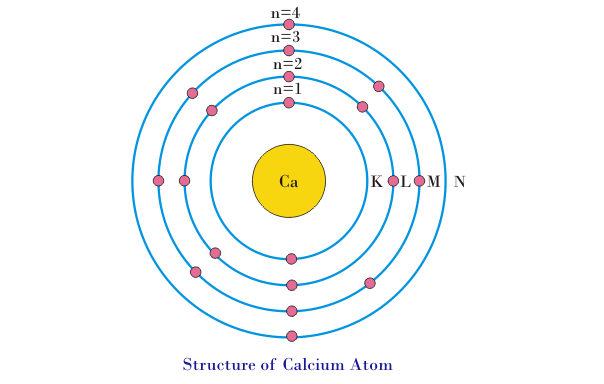
- 最外层能量水平的电子称为“价电子”。“价电子”的最大可能数量为8.如果最外面轨道中的电子数为8,则原子变得稳定。其原子在其最外壳(轨道)中自然具有8个电子的材料,不会与其他材料反应。惰性气体如氦气,氖,氩,氪等完全填充的外壳,因此不会与其他材料反应。
- 原子的“价电子”与细胞核松散地束缚,并且可以通过不同的方法来释放/除去通过加热,通过施加电压等。
- “价电子”形成将材料原子保持在一起的键合。材料的大部分性质由这些材料中的这些键决定。
- 每个主壳(能级)被细分为子壳。这些子外壳称为轨道。这些子壳/轨道由S,P,D,F等指定量子数,L = 0,1,2,3,4,......(n-1)等。任何主壳中的子壳数等于主量子数为'n'。通过添加子壳的电子容量,可以确定任何主壳的电子容量。子壳的最大电子容量由2(2L +1)的公式控制。子壳的容量在下表中给出 -
| SL。没有。 | 亚层 | 量子数(L) | 亚电子层的电子容量 2(2L + 1) |
| 1 | S. | 0. | 2(2×0 + 1)= 2 |
| 2 | P. | 1 | 2(2×1 + 1)= 6 |
| 3. | D. | 2 | 2(2×2 + 1)= 10 |
| 4. | F | 3. | 2(2×3 + 1)= 14 |
- 第一壳层,即K壳层,有主量子数1和一个s轨道,因此s轨道记作1s。
- 第二壳即,L壳将具有主要量子数2,并且将具有一个s和一个p轨道,它们分别表示为2s和2p。
- 第三壳I.E.M壳将具有主量子数3并且将具有一个S,一个p和一个d轨道,它们分别表示为3s,3p和3d等。
- 在这里,我们还有另一件事要记住,S轨道有一个亚孔,每个亚轨道可以包含最大两个电子。p orbital有3个子孔和d orbital有5个子孔。
- 首先填充较低的能量子孔,然后填充下一个更高的轨道。在其下轨道下完成之前,不会有任何填充任何更高的眶内或亚坏岩体的机会。
如果我们经过下面的示例,它将很清楚我们。
具有13个电子的铝的原子结构
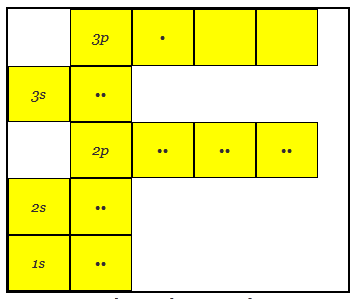
具有29电子的铜的原子结构
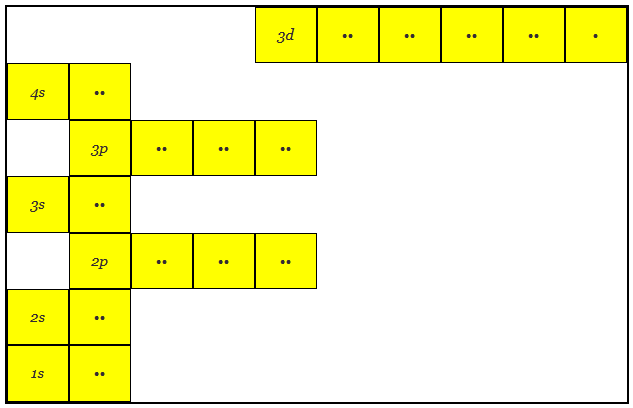
在这里,可以注意到3D轨道处于比4s更高的能量水平
具有47个电子的银原子结构
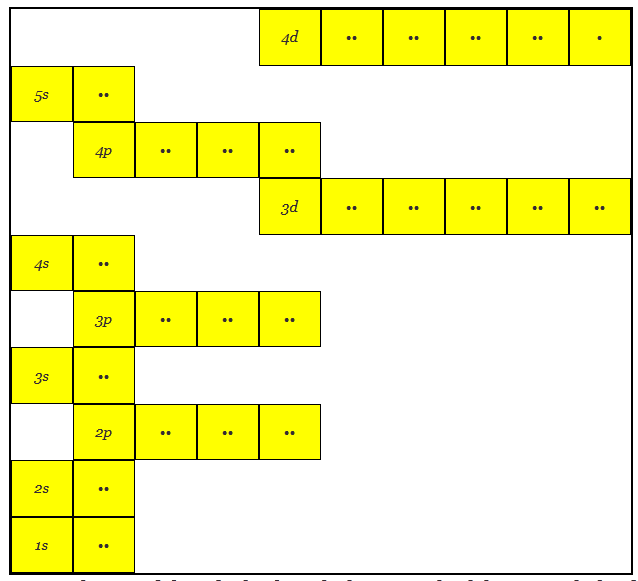
这里可以注意到,3D轨道在较高的能量水平上,类似于4D轨道在较高的能量水平上比5s类似。
现代原子理论
现代原子理论比道尔顿的理论更加进化。现代原子理论也被称为量子理论。这个概念波粒子二元性这里进入图片。它说认为是颗粒的电子有时可以表现波。因此,原子具有由概率云包围的核。这些云是电子的最可能位置。这些云的尺寸和形状可以通过使用波的方程来计算。









